本文所述医疗器械“三证”是指医疗器械的注册证、生产许可证、经营许可证,是用于证明医疗器械注册、生产、经营三方面均合法的资质材料。实践过程中发现,对于不同类别的医疗器械其资质内容和要求有所不同,正确认识医疗器械的类别和资质要求,有利于采购供应人员更高效准确的完成资质审核,确保医疗器械的合法性和安全性。本文通过查询国家相关法律法规,结合实际工作经验,简单总结了医疗器械的资质内容和要求,为医工同行提供参考。
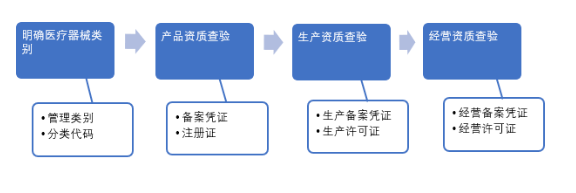
医疗器械资质审核,首先要明确医疗器械的管理类别和分类代码,然后根据类别有针对性的审核产品资质、生产资质以及经营资质。
01、产品资质
根据新版《医疗器械监督管理条例》、《医疗器械注册与备案管理办法》,医疗器械按风险程度由低到高分为一、二、三类。第一类医疗器械需办理医疗器械备案凭证,第二类、第三类医疗器械需取得医疗器械注册证。正确识别医疗器械注册证号码,可确认其管理类别、分类代码、审批单位等多种信息。具体情况见下表:
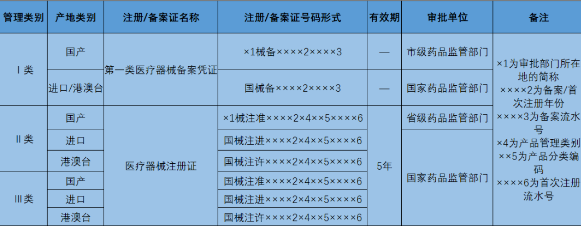
应当重点审核审批机构是否与产品的管理类型相符、确认证上规格型号等内容符合产品实际情况、确认注册证有效期等,存在产品信息变更时,还应当审查该产品注册证所附的医疗器械变更注册文件。
该产品注册证所附的医疗器械变更注册文件。
02、生产资质
根据新版《医疗器械生产监督管理办法》,从事第二类、第三类医疗器械生产活动,应当取得医疗器械生产许可证;从事第一类医疗器械生产活动,应当办理医疗器械生产备案凭证。因此需根据医疗器械类别查验生产厂家的生产备案凭证或生产许可证。相关内容如下表:
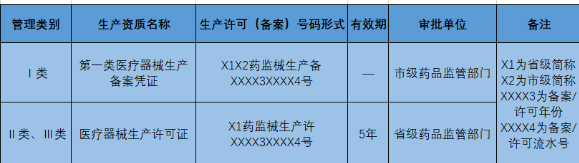
对生产资质要重点核查生产范围内是否包含采购的医疗器械的分类编码、许可证号、产地等信息与产品实际包装相符,并且许可证处于有效期内。
2022年5月1日施行的新版《医疗器械生产监督管理办法》取消了生产登记表,所以5月1日之后下发的生产许可证不再附带生产登记表。但5月1日之前批准的尚未过期的生产许可证仍然有效,应当附有生产登记表,需审核登记表中是否包含所购产品注册证号。

03、经营资质
根据新版《医疗器械经营监督管理办法》,经营第三类医疗器械实行许可管理,经营第二类医疗器械实行备案管理,经营第一类医疗器械不需要许可和备案。生产厂家销售自己注册的医疗器械无需办理经营资质。因此,要根据器械的类别审核供应商对应的经营资质。
资质审核时,对于第一类医疗器械经营企业和直售自家产品的生产厂家无需经营资质。第二类医疗器械需审核其经营备案凭证,第三类医疗器械需审核其经营许可证,应当重点关注经营备案凭证和经营许可证上的经营范围应该包含所采购的医疗器械分类代码,同时确保经营许可证在有效期内,避免经营范围不符、许可过期的情况。
许可过期的情况。04.
04、注意事项
1、证照电子化
国家及地方相关部门已逐步推广医疗器械注册证、生产许可证、经营许可证的电子化。电子证照与纸质版证照在内容上无异,两者具有同等的法律效力,通常电子证上标有二维码,可扫码在线验证,并且电子证照可实现联网共享查询等功能。对于资质审核人员而言,应当转变传统的审查思路与方法,在适当时候摆脱对纸质证件的依赖,充分利用电子证书的便捷性,通过网络查询、扫描验证等方式快速验证资质的真伪,提升工作效率。
2、多证合一
基于深化“放管服”改革背景,各地政府纷纷出台了“多证合一”政策。多证合一的证照,只需一张证照便可审查多种资质,极大减轻了审核人员的工作量。由于各地政府出台的相关政策有所不同,在实际工作中如果遇到“多证合一”的情况,应当结合当地政策进行确认,下面以重庆、上海为例进行分析。
①根据《渝府办发〔2017〕158号意见》, 2018年6月30日起,重庆的经营企业可自愿将第二类医疗器械经营备案凭证整合到营业执照中去,整合之后的备案凭证不再单独发放。针对这类选择证照整合的经营企业,经营项目直接标注在营业执照的经营范围上。可通过扫描营业执照上的二维码进入国家企业信用信息公示系统(www.gsxt.gov.cn)“多证合一”公示栏查询确认。
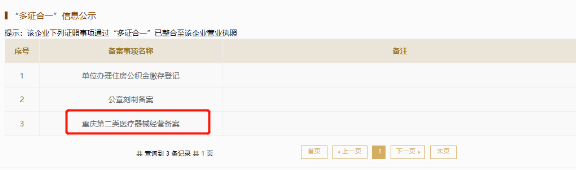
②根据《沪药监械管〔2019〕92号通知》,2019年12月1日起,上海的经营企业可在多种情况下将第二类经营备案、第三类经营许可证进行合并办理,批准后只下发医疗器械经营许可证,许可证上添加备注栏注明“备案凭证号、二类备案经营范围”等内容,作为第二类医疗器械经营备案的凭证。 所以针对这类企业,资质审核时不再要求单独提供经营备案凭证。

结束语
医疗器械资质审核是一项非常严谨、细致的工作,具有专业性、严肃性、程序性等特点,医工部门审核人员应该不断学习相关的最新法规政策,熟练掌握资质审核的最新要求,强化过程管理,确保所采购的医疗器械合法合规、安全有效,最大限度规避风险隐患。
随着证照电子化的推广、“多证合一”等政策实施,资质管理人员应该转变思维,更新观念,思考如何利用互联网、信息技术等手段提升医疗器械资质审核工作的科学化和规范化,提高资质审核质量和效率。